JMC|突破性MAT2A 抑制剂:2 (1H)-喹喔啉酮衍生物
甲硫氨酸腺苷转移酶2A(MAT2A)已成为一种合成致死性药物靶点,用于治疗携带甲基硫腺苷磷酸化酶(MTAP)基因纯合缺失导致的癌症。尽管在MAT2A 抑制剂的发现与开发方面已取得显著进展,但目前关于这些化合物对MTAP缺陷型癌症的选择性的理解相对有限。提高MAT2A抑制剂对MTAP缺陷型癌症的选择性仍是一项重大挑战。
2025年1月6日,中国科学院上海药物研究所黄敏课题组与中国药科大学查晓明课题组合作,在JMC期刊上发表了题为“Discovery of 2(1H)-Quinoxalinone Derivatives as Potent and Selective MAT2A Inhibitors for the Treatment of MTAP-Deficient Cancers”的论文。
研究团队通过基于结构的药物设计及系统的构效关系(SAR)探索,发现了一系列以2(1H)-喹喔啉酮为骨架的新型MAT2A抑制剂。其中,化合物28对MAT2A的酶活性展现出良好的抑制活性,且在杀伤MTAP缺陷型癌细胞方面具有显著提高的选择性。化合物28在MTAP缺陷型肿瘤模型中也显示出良好的药代动力学特性和改善的体内抗癌活性。这些研究结果为高选择性MAT2A抑制剂的发现与开发指明了新方向。
研究成果
1. MAT2A抑制剂行业发展情况
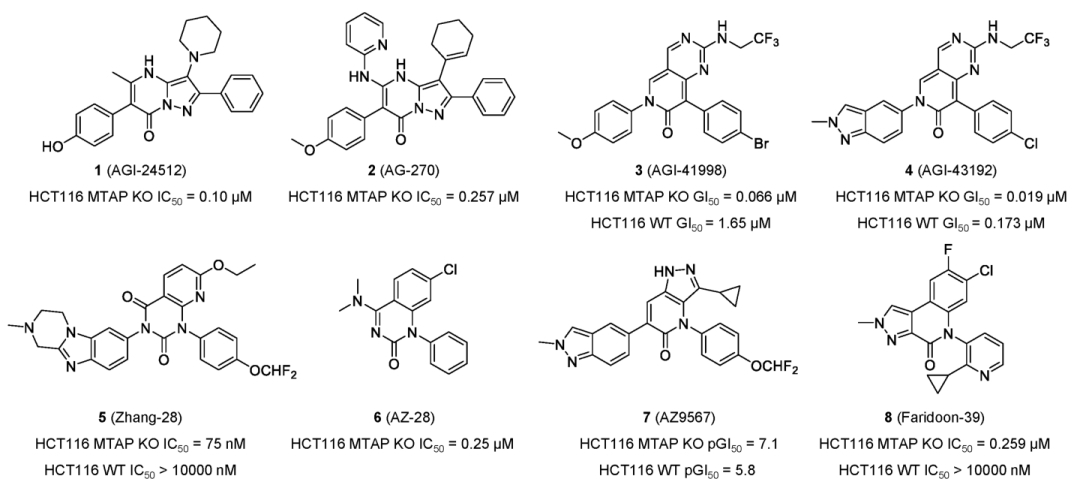
Agios公开了其先导化合物AGI-24512(1)和临床候选化合物AG-270(2)。然而,AG-270的临床研究于 2023年终止。另一系列具有不同化学骨架的化合物促成了AGI-41998(3)和AGI-43192(4)的发现。此外,与3相关的Zhang-28(5)也表现出高抗肿瘤效力。阿斯利康还报告了通过基于片段的药物发现AZ-28(6),并且一系列吡咯并吡啶酮化合物的进一步药物化学优化产生了AZ9567(7)。此外,zui近报道的一种具有吡唑并 [3,4-c]喹啉-4-酮骨架的化合物(8)表现出高选择性和体内liao效。目前,三种MAT2A抑制剂,IDE397(NCT04794699)、S095035(NCT06188702)和 ISM3412(NCT06414460),已进入I期临床试验。
图1. 代表性MAT2A抑制剂的化学结构
2. 化合物28的发现
1)药物设计
目前MAT2A抑制剂主要是通过与位于MAT2A/MAT2B 复合物界面的变构位点相结合来研发的(图2A)。化合物3与MAT2A结合的晶体结构(PDB: 7RWH)表明,化合物3的羰基与MAT2A的精氨酸313残基形成直接氢键相互作用,而其甲氧基苯基则与甘氨酸193形成氢键相互作用(图2B)。甲氧基苯基向外延伸至MAT2A 的变构口袋,这表明在溶剂暴露区域有进一步修饰的可能性。
骨架跃迁策略是药物设计领域中一种常见且有效的重要方法。作者通过将溴苯、甲氧基苯和三氟乙胺连接到7 (8H)-蝶啶酮核心结构上,研制出了化合物9(图2C)。随后检测了该化合物对MAT2A 的抑制活性,以及对 MTAP 基因完整(B16F10 MTAP WT)或敲除(B16F10 MTAP KO)的同基因细胞对的抗增殖活性。与 AGI-41998 相比,化合物9保留了对 MAT2A 的抑制活性,半数抑制浓度(IC50)为150.6 nM,并且与野生型细胞相比,对MTAP 敲除细胞具有一定的选择性[选择性指数(SI)>3.1]。然而,我们发现它对 B16F10 MTAP KO 细胞生长的抑制活性显著降低(IIC50 = 6.54 μM)。
图2. 新型MAT2A抑制剂的合理设计
(A) 位于MAT2A/MAT2B 复合物界面的变构位点(PDB: 4NDN);
(B) MAT2A 与AGI-41998 结合的晶体结构(PDB: 7RWH);
(C) 新型 MAT2A 抑制剂骨架的设计方法。
作者接下来对一系列7(8H)-蝶啶酮衍生物进行了评估优化,结果发现化合物20对MAT2A具有较强的抑制活性,且对MTAP基因敲除的癌细胞系具有较高的抗增殖选择性。进一步的骨架筛选和构效关系探索,使研究团队发现了化合物28,这是一种以2(1H)-喹喔啉酮为骨架的新型 MAT2A抑制剂。
2)化合物28与MAT2A的结合方式
通过分子对接研究了化合物28与MAT2A的结合模式。以化合物3与MAT2A结合的晶体结构(PDB: 7RWH)作为模拟模板。与MAT2A的分子模拟表明,化合物28占据了 MAT2A的变构位点,这与化合物3类似(图3A)。2 (1H)-喹喔啉酮核心能够与精氨酸313形成氢键相互作用,并与苯丙氨酸18残基形成π-堆积相互作用,这些被认为是与MAT2A的关键相互作用(图3B)。该模型还表明,OCF₂H与甘氨酸275的羰基之间可能存在氢键相互作用。此外,化合物28的1-甲基苯并咪唑位于口袋外部,可与谷氨酰胺190残基的侧链形成芳香相互作用。3位的氮原子有可能与甘氨酸193形成氢键相互作用,而氮原子上的甲基取代基以及2位碳原子延伸到溶剂暴露区域。
图3. 通过分子对接揭示的化合物28在MAT2A变构口袋上的结合模型(PDB: 7RWH)。
(A)化合物28的结合构象;
(B)化合物28与MAT2A之间的潜在相互作用。
3)构效关系
基于目标化合物的生物活性,图4直观地总结了整体的构效关系。观察到骨架和取代基对化合物的酶活性和选择性有不同的贡献,这为进一步优化提供了思路。
图4. 构效关系分析
3. 化合物28的强效和高度选择性
1)对MTAP缺失型和野生型癌细胞的选择性
测试表明化合物28对MTAP缺失型细胞表现出强大的抗增殖活性,且其在MTAP 缺失型和野生型细胞之间的选择性与 AGI-24512 相当(图5A)。为进一步确认,在 MTAP 缺失的 MIA PaCa-2 细胞中过表达 MTAP。由于蛋白质精氨酸甲基转移酶5(PRMT5)活性受损,MTAP 缺失的替代标志物——对称二甲基精氨酸(SDMA)在 MTAP 表达时增加(图5B)。与此同时,化合物28的抗癌活性降低(图5C)。此外,发现在 MTAP 敲除的 B16F10 细胞中补充 MTAP 可逆转化合物28的抑制活性,而酶失活的 MTAP-D220A 突变体对其无影响(图5D、E)。这些数据有力地支持了化合物28的抗癌活性与 MTAP 缺失密切相关。
图5. 化合物28选择性抑制 MTAP 缺失型癌细胞系的增殖
(A)化合物28、AGI-41998 和 AGI-24512 在一组 MTAP 缺失型和野生型(WT)癌细胞系中的 pIC50 值;(B) 对稳定过表达 MTAP 或其空载体的 MIA PaCa-2 细胞中 SDMA 和 MTAP 水平的免疫印迹分析;(C) 化合物 28 在(B)中所述的 MIA PaCa-2 细胞对中的增殖抑制活性;(D) 对B16F10 细胞组中 SDMA 和 MTAP 水平的免疫印迹分析。在 MTAP 敲除的 B16F10 细胞中表达 MTAP - WT、MTAP - D220A 突变体或空载体。以亲本细胞(NC)作为对照;(E) 化合物28在(D)中所述的 B16F10 细胞组中的增殖抑制率。用一系列浓度的化合物28处理细胞96小时。
2)对细胞内SAM和SDMA水平的影响
为证实化合物28对细胞靶点的抑制作用,研究人员对细胞内S-腺苷甲硫氨酸(SAM)和对称二甲基精氨酸(SDMA)的水平进行了检测。结果表明化合物28能有效阻断 MAT2A 在细胞内的酶活性。
图 6. 化合物28在MTAP 缺失或野生型的 MIA PaCa-2 和 B16F10 细胞对中的细胞活性。MTAP 缺失的 MIA PaCa-2 细胞稳定表达 MTAP 或空载体作为对照。在 B16F10 细胞中敲除 MTAP。
(A,B) 用所示浓度的化合物28处理4小时后,相对SAM 水平;
(C,D) 用所示浓度的化合物28处理48小时后,对SDMA 和 MTAP 水平的免疫印迹分析。
3)化合物28优先在MTAP基因敲除细胞中诱导DNA损伤
阻断 MAT2A 依赖的甲硫氨酸分解代谢会诱导癌细胞发生 DNA 损伤。因此,通过免疫印迹和免疫荧光染色测定来检测 γH2AX 的水平,γH2AX 是 DNA 双链断裂(DSB)的可靠替代标志物。如图7 所示,在用化合物 28 和参考化合物 AGI-41998 处理后,仅在 SF126 MTAP 基因敲除细胞中观察到 γH2AX 水平显著增加,而在 SF126 MTAP 野生型细胞中仅观察到 γH2AX 有轻微增加。与 AGI-41998 相比,经化合物28处理后,MTAP 野生型和基因敲除细胞之间的差异更为明显。这些结果表明,由化合物28介导的对 MAT2A 的抑制所引发的DNA损伤,可能是其在 MTAP 缺陷细胞中发挥抗癌活性的原因。
图7. 化合物28在 SF126 MTAP 基因敲除和野生型细胞中诱导的 DNA 损伤。细胞用指定浓度的化合物28或 AGI - 41998 处理96小时。
(A) 蛋白质免疫印迹分析;
(B,C) 免疫荧光分析的定量分析及代表性图像。比例尺,25微米。
4)理化性质分析与初步药代动力学研究
药代动力学研究表明,化合物28呈现出良好的药代动力学特征,具有较高的血浆药物暴露量和口服生物利用度。
5)对细胞系来源的异种移植瘤的体内抗肿瘤作用
化合物28能显著降低肿瘤中SAM的水平,并且在MTAP 缺失的MIA PaCa - 2 和 DAOY 异种移植瘤模型中表现出显著的抗肿瘤效果。
图 8. 化合物28在 MIA PaCa - 2 异种移植瘤模型中的体内疗效
(A) 为期28天治疗期间的肿瘤生长曲线;
(B) 28天治疗终点时的肿瘤重量变化。
图9. 在最后一次给药后的指定时间,对 MIA PaCa - 2 异种移植瘤模型进行体内药效动力学(PD)分析
(A) 血浆中SAM的浓度;
(B) 肿瘤中SAM的浓度;
(C) 对以60mg/kg剂量的化合物处理后的肿瘤中SDMA 水平进行免疫印迹分析。
图10. 化合物28 在 DAOY 异种移植瘤模型中的体内疗效
(A) 肿瘤生长曲线;
(B) 肿瘤重量变化;
(C) 血浆中的药物浓度;
(D) 对肿瘤中对称二甲基精氨酸(SDMA)水平的免疫印迹分析。
总结
该研究通过基于结构的药物设计及系统的SAR探索确定了一种新型 MAT2A 抑制剂,其对 MTAP 缺陷型癌症具有出色的抗肿瘤活性和高度选择性,为进一步设计抑制 MAT2A 的药物,挖掘其在 MTAP 缺陷型癌症治疗中的潜力奠定了基础。
MAT2A蛋白表达及结构解析
「青云瑞晶」已完成MAT2A的蛋白表达和结构解析,基于这些实验条件和库存蛋白,青云瑞晶将项目的交付时间缩短至1-2个月,并确保项目的成功交付。
实验结果展示:蛋白纯化结果
实验结果展示:蛋白纯化结果
「青云瑞晶」提供专业的结构解析技术服务,自拥有单晶X射线衍射(XRD)、冷冻电镜单颗粒法(CryoEM-SPA)、MicroED 三种结构解析技术平台,根据蛋白质的不同性质,提供不同的解决方案,结合精良高端的实验设备、经验丰富的高学历科研团队,为您提供从蛋白表达开始的一站式结构解析服务,灵活多样化满足您的多种科研及工业界需求。